Deneyin Amacı:
Tuzlu suyun elektrik
akımı ile tuz ve suya ayrılmasını görebilmek.
Düşünce Soruları?
1.
Metallerin farklı metallerle nasıl kaplandığını araştırınız.
Araç ve Gereçler: kömür elektrot, su, beherglas,
tuz, güç kaynağı, bağlantı kablosu
Uygulama:
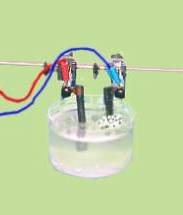
1. Yandaki
düzeneği hazırlayalım.
2. Beherglası
üçte iki oranında tuzlu su koyunuz ve kömür elektrotları suya
daldırınız.
3. Kömür elektrotlar birbirine değmeyecek şekilde
sabitleyelim.
4. Elektrotları bağlantı kabloları ile elektrotlara
bağlayalım.
5. Elektrotlara
akım vererek gözlemleyelim.
|
 |
|
|
|
|
Değerlendirme Yapalım:
Yemek tuzunun (NaCl-Sodyum klorür)
elektrolizinde su içinde gaz açığa çıkar. Bu gaz içinde hidrojen ve klor
molekülleri bulunur. Kloru kokusundan tanıyabilirsiniz. Sodyum (Na)
elementi ise dibe çöker.
Kimyasal olayın denklemi;
NaCl →
Na+ + Cl- olur.
Bilgilenelim:
İletken bir çözeltiden elektrik
akımı geçirmek suretiyle bir bileşiğin, kendisini oluşturan elementlere
ayrılması olayına “elektroliz” denir.
Sulu çözeltileri elektrik akımını geçiren çözeltilere “elektrolit
çözeltilere” denir. Asit, baz ve tuz çözeltileri elektrolit
maddelerdir. Şeker, benzinin sulu çözeltileri ise elektrik akımını iyi
iletmediklerinden elektrolit çözelti değildir.
Elektroliz sırasında ortaya çıkan ürünlerin miktarı akım şiddetine de
bağlıdır. Akım şiddeti arttıkça genellikle daha hızlı bir şekilde
element oluşur.
Çözeltideki (+) yüklü iyonlara “katyon” , (-) yüklü iyonlara da “anyon”
denir. Kimyasal reaksiyonlarda +) yüklü iyonlar katot, (- ) yüklü
iyonlar da anot tarafında toplanır.
www.fencebilim.com - Hidayet
TERECİ
|



