|
|||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||
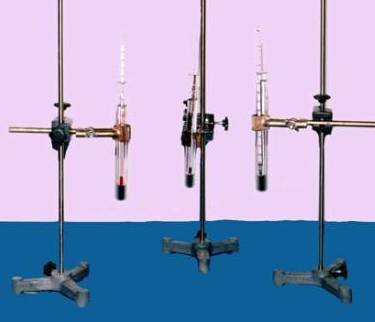
KİMYASAL REAKSİYONLARDA ISI ALIŞVERİŞİNİN GÖZLENMESİ |
|||||||||||||||||||||||||||||||
Dikkat: Asit tehlikeli (yakıcı ve delici) bir bileşik olduğu
için deney gözlüğü, plastik eldiven ve önlük kullanınız. Asit üzerine su
dökmeyiniz.
1.
Çevrenizde ısı veren kimyasal olay oluyor mu?
Değerlendirme Yapalım: Sodyum hidroksit (NaOH) ile hidroklorik asidin (HCl) birleşmesi sonucu tuz ve su oluşur. Bu reaksiyon ekzotermik (ısı veren) bir reaksiyondur. Yaptığınız deneyde bulduğunuz sıcaklık artışı, açığa çıkan ısı enerjisini gösterir.
Bilgilenelim: Kimyasal reaksiyonlarda maddeler birbirleriyle etkileşerek yeni ürünler oluştururken ya çevrelerine ısı verirler (ekzotermik reaksiyonlar) ya da çevrelerinden ısı alırlar (endotermik reaksiyonlar ). Günlük hayatta en çok ekzotermik reaksiyonlarla karşılaşırız. Ekzotermik olaylarda sistemin enerjisi azalır. Tüm yanma olayları, oksitlenme olayları 8demirin paslanması), kimyasal bağ oluşumu, gazların suda çözünmesi, asit ve bazların etkileşmesi ekzotermik reaksiyonlardır. Aşağıdaki örnekleri inceleyiniz.
- C (Karbon) + O2 (Oksijen)
------- CO2 (Karbondioksit) + Isı
Siz Deneyin: Hidroklorik asit (HCl) ile amonyağı
(NH3)
bileşiklerini belirli oranda birbiri ile karıştırınız. Asit ve baz
karıştığında ısı açığa çıkacaktır. Yukarda yapılan işlemleri
tekrarlayınız. Tüpün sıcaklığının arttığını elinizle hissediniz. |
|||||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||||