|
|||||||||||||||||
|
|||||||||||||||||
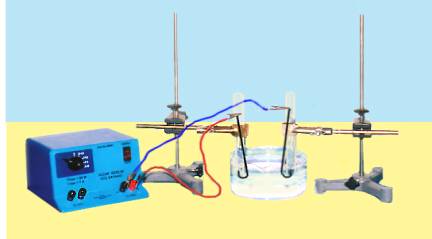
SUYUN KİMYASAL YOLLA (ELEKTROLİZ) ELEMENTLERİNE AYRILMASI |
|||||||||||||||||
Deneyin Amacı:
Su bileşiğinden
elektrik enerjisi kullanılarak saf elementleri elde edilmesi. 1.
Gündelik yaşamda kullandığımız bileşiklere örnekler verebilir misiniz?
Değerlendirme Yapalım:
Suyun elektrolizinde; (-) kutba
bağlı olan tüpte iki hacim hidrojen, (+) kutba bağlı olan tüpte bir
hacim oksijen gazı toplanır.
Patlayarak yanan
tüpte hidrojen gazı (yanıcı gaz)birikmiştir. Kibritin alevini daha
parlak yakan tüpte ise gaz ise oksijen (yakıcı gaz) gazı vardır. Elektroliz düzeneğinde pozitif ve negatif kutupların her ikisine birden “elektrot” denir. Güç kaynağının pozitif kutbuna bağlanan elektrot “anot” , negatif kutbuna bağlanan ise” “katottur”. İki kutup arasında elektrik taşınmasını sağlayan iletken çözeltiye “elektrolit” denir. Suyun elektrolizinde katotta (-) “hidrojen" elementi, anotta (+) ise "oksijen" elementi toplanır. Deney sırasında bir süre sonra tüplerde toplanan hidrojen gazı hacim olarak oksijen gazının iki katı olur. Suyun formülü H2O olduğu için tüplerde biriken gaz oranları 2 ye 1 olur. Siz Deneyin:
Başka hangi bileşikleri elektroliz yöntemi ile elementlere
ayırabilirsiniz? Araştırıp deneyiniz? |
|||||||||||||||||
|
|
|||||||||||||||||